A Agência Nacional de Vigilância Sanitária (Anvisa) encaminha uma regulamentação do medicamento Zolgensma, usado contra a Atrofia Muscular Espinhal (Ame).
Continua depois da publicidade
A informação foi repassada por servidores da Anvisa ao deputado estadual de Santa Catarina Fabiano da Luz (PT) na manhã desta sexta-feira (14). Segundo o parlamentar, a Anvisa assinou um termo de compromisso com a empresa farmacêutica que produz o medicamento e a regulamentação deve ser publicada até a quarta-feira da próxima semana no Diário Oficial da União (DOU). Um técnico da Anvisa informou à reportagem que a análise técnica do caso foi concluída e que o processo “está em etapa de publicação”.
A assessoria da Anvisa confirmou que o pedido de registro do medicamento está em fase final de análise. O órgão informou que novas informações de segurança sobre o medicamento foram enviadas no último dia 22 de julho e que o processo segue “em análise prioritária pela Agência para finalização dos termos de compromissos” com a empresa responsável pelo pedido de registro da medicação no país.
Com a regulamentação, o tratamento de crianças com Ame que precisem do medicamento poderá ser feito no país. Até agora, as crianças precisavam ir aos Estados Unidos, onde o remédio já havia sido aprovado, para passar pelo tratamento. A regulamentação não significa, no entanto, que o medicamento estará disponível pelo SUS.
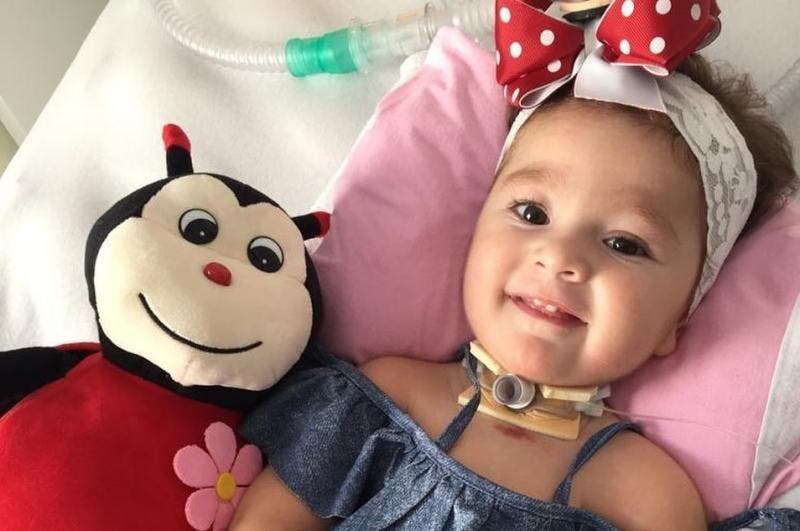
Foi o caso da menina Antonella Garcia Cunha Moro, de Blumenau, que embarcou em fevereiro deste ano para receber o medicamento nos Estados Unidos. O tratamento só foi possível por causa de uma campanha de seis meses que arrecadou mais de R$ 11 milhões em doações para custear a aplicação do Zolgensma.
Continua depois da publicidade
O medicamento é conhecido como o mais caro do mundo, é alvo de algumas controvérsias e ainda aguardava a autorização da Anvisa para comercialização no país. A empresa fabricante do medicamento deve acompanhar a evolução de todas as crianças submetidas ao tratamento por 15 anos. A aplicação da dose também deverá ser feita de forma controlada desde a saída do laboratório até a aplicação na instituição de saúde.
O medicamento precisa ser aplicado nas crianças com Ame até os dois anos de idade e já teria proporcionado evoluções nas crianças que fizeram o tratamento com ele como dispensar o respirador e, em alguns casos, até mesmo sentar e caminhar.
– É um avanço muito importante. Primeiro, porque as crianças que precisam dele não precisam mais ir aos Estados Unidos, fazer passaporte, visto, ficar vários dias lá. E segundo porque agora, com a regulamentação, podemos passar a pleitear que esse medicamento seja fornecido pelo SUS – avalia o deputado Fabiano da Luz, que é autor de dois projetos sobre o tema na Assembleia Legislativa.
> Saiba como proteger as crianças durante pandemia de coronavírus